Die Zusammenarbeit mit Forschungsgruppen aus Heidelberg, Forscher von der Charité – Universitätsmedizin Berlin erläutert die neuartige Krankheit Prozesse, die bei der Entwicklung der Lungenfibrose. Sie konnten zeigen, dass das protein, bekannt als NEDD4-2 spielt eine wichtige Rolle bei Lungen-Gesundheit und dass der Verlust dieser entscheidende regulatorische Molekül hat erhebliche Auswirkungen auf die verschiedenen Mechanismen, die in der Entwicklung der chronisch fortschreitende Lungenerkrankung. Diese neuen Erkenntnisse machen es einfacher, weiter zu untersuchen, die genauen Mechanismen bei der Entstehung und progression der Lungenfibrose. Die Ergebnisse der Forscher, wurden veröffentlicht in Nature Communications, wird es den Wissenschaftlern ermöglichen, neue therapeutische Ansätze zu entwickeln.
Lungenfibrose ist eine ernste Lungen-Erkrankung, die hauptsächlich ältere Menschen betroffen sind; es gibt praktisch keine wirksamen Behandlungen. Die Krankheit ist gekennzeichnet durch progressive Gewebeveränderungen führen zu Vernarbung der Lunge. Jedoch, seine Ursachen sind weitgehend unbekannt, und die zellulären Mechanismen, die in Ihrer Entwicklung bleiben schlecht verstanden. Der Begriff „mukoziliären clearance“ bezieht sich auf einen selbstreinigenden Mechanismus, beruht auf der ciliated Zellen in das Epithel der Lunge treibt eingeatmete Krankheitserreger und andere Partikel, gefangen im Schleim aus den Atemwegen. Wir wissen, dass die Veränderungen im Epithel assoziiert sind mit der Produktion von überschüssigem Schleim. Sie sind auch im Zusammenhang mit der beeinträchtigten clearance von diesem Schleim und seine primäre strukturelle Komponenten (bekannt als ‚Schleimstoffe‘). NEDD4-2 ist involviert in den Abbau von einer Reihe anderer Proteine, die wiederum sind dafür verantwortlich, diese Prozesse zu regulieren, Lungen-Epithel-Funktion. Dies bedeutet, dass NEDD4-2 ist ein schlüsselprotein, das mit einer zentralen Rolle in der Pathogenese der Lungenfibrose.
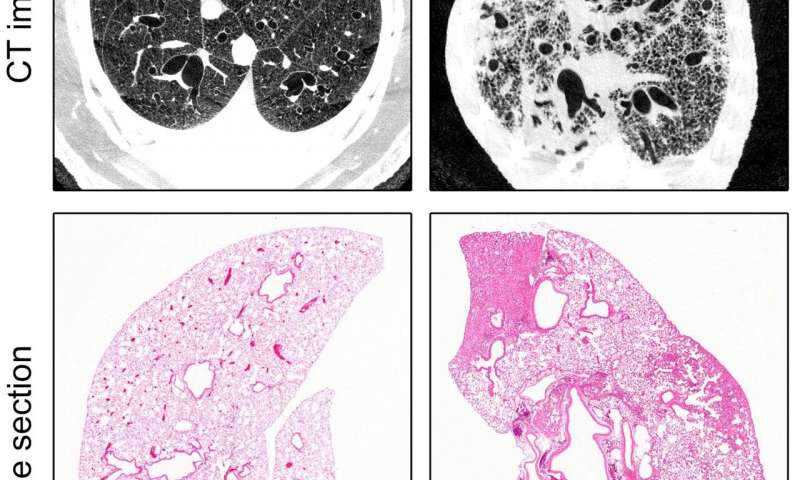
Die Zusammenarbeit mit Kolleginnen und Kollegen aus dem deutschen Zentrum für lungenforschung (DZL), das Universitätsklinikum Heidelberg und das Deutsche Krebsforschungszentrum, das team von Forschern unter der Leitung von Prof. Dr. Marcus Mall (Direktor der Charité-Abteilung für Pädiatrische Pulmologie, Immunologie und Kritische Medizin und Professor am Berliner Institut für Gesundheit [BIH]) gelang die Entwicklung einer neuartigen Tiermodell der idiopathischen pulmonalen Fibrose (IPF). Da NEDD4-2 ist entscheidend für die frühe Entwicklung, die Forscher erst gelöscht wird, die entsprechenden kodierenden Gens in lungenepithelzellen einmal hatten sich die Tiere Erwachsenenalter erreicht. Die Wissenschaftler untersuchten die Tiere, sobald Sie hatte ein Stadium erreicht, in etwa vergleichbar zu dem Punkt, an dem die Krankheit diagnostiziert werden, in einem menschlichen Patienten. Sauerstoff-Sättigungs-Messwerten, die in dieser Phase zeigte ein Niveau der Lungenfunktion Beeinträchtigung, die charakteristisch für die Krankheit. Mithilfe von Gewebeschnitten und CT-Bildgebung zu untersuchen, die Lunge, die Forscher fanden auch Beweise lückenhaft Narbenbildung, eine Art von strukturellen Anomalien, die Indikativ für die Fibrose. Fanden die Forscher weitere Hinweise für die Bedeutung von NEDD4-2 in der Pathogenese der IPF: Lungen-Gewebe-Biopsie-Proben von Patienten mit IPF enthielten signifikant geringere Mengen der beiden Transkripte und Proteine. Mittels Massenspektrometrie haben die Forscher führten dann, was ist bekannt als „protein-profiling“ – eine Analyse der Gesamtheit aller Proteine in der Lunge produziert. Dabei zeigte sich eine hohe überschneidung zwischen den Proteinen gefunden werden, anders ausgedrückt in der Lunge von Patienten mit IPF und in den Tieren in dieser Studie verwendet. „Unsere Ergebnisse können den Forschern helfen, weiter zu untersuchen, die Pathogenese und progression dieser Lungenerkrankungen und die Entwicklung neuer Behandlungen. Dieses Modell könnte sich als nützlich erweisen für die präklinische Testung von Substanzen mit therapeutischem potential, oder zur Entwicklung von Markern für die Früherkennung der Krankheit“, sagt Prof. Mall.
Bei der Untersuchung der zugrunde liegenden krankheitsmechanismen, die Forscher entdeckten, dass geringere Mengen von NEDD4-2 in Epithelzellen Ergebnis in epithelialen Umbau der Atemwege. Nicht nur sind die verschiedenen Zelltypen in unterschiedlichen Proportionen, die Zellen auch produzieren erhöhte Mengen bestimmter Schleimstoffe. In Kombination mit Veränderungen in der epithelialen Natrium-transport und die daraus resultierende Verringerung des Volumens der airway surface liquid, führt dies zu einer Beeinträchtigung der mukoziliären clearance. Mangel von NEDD4-2 bewirkt auch eine erhöhte Aktivität des TGFß-Signalwegs, das fördert die Bildung von Fibrose. Fasst man die Ergebnisse der Studie, die Studie der erste Autor, Dr. Julia Dürr, der sagt: „Dies bedeutet, dass wir feststellen konnten, dass ein Mangel an NEDD4-2 ist direkt verbunden mit der mukoziliären Dysfunktion und Störungen des TGFß-Signalwegs. Nach heutigem Stand des Wissens, beide spielen eine Rolle in der Pathogenese der IPF.“
