
Alzheimer-Krankheit ist die führende Ursache der Demenz weltweit und eine Hauptursache von Behinderung. Nun, Forscher an der Universität von Osaka und Hokkaido University haben gezeigt, dass wiederholte Niederschläge-Auflösung Veranstaltungen von Salz-Kristallen treten auch bei geringen Salz-Konzentrationen in nanoscales, und dass es beschleunigt die aggregation der neurotoxischen amyloid-β-Peptide Verwicklung in die Pathogenese.
Das menschliche Gehirn besteht aus etwa 86 Milliarden Nervenzellen, ungefähr so viele Sandkörner wie in einer großen dump truck. Diese Neuronen jonglieren Elektrochemische Informationen als Signale zwischen Gehirn, Muskeln und Organe, um zu instrumentieren der Symphonie des Lebens aus dem das überleben selbst-Bewusstsein. Die Alzheimer-Krankheit stört das komplexe neuronale Netzwerk, wodurch funktionelle Behinderung und Zelle Tod. Noch uncurable, verfügbare Behandlungen werden eine symptomatische, unterstützende oder palliative; ein Durchbruch im Verständnis Ihrer Pathogenese kann erhellen sich die Aussichten für Medikamente, Diagnostik und Prävention.
Die Rolle von amyloid bei Alzheimer-Krankheit ist lang erkannt worden. Amyloid-β-Peptide sind abgeleitet von amyloid-precursor-protein, und Sie selbst zusammensetzen, in den Größen von low-molecular-weight Aggregate und größere oligomere amyloid-Fibrillen. Diese letzten sind bekanntermaßen neurotoxischen aber neue Forschung schlägt vor, dass oligomere ungeordnete Aggregate sind auch giftig, möglicherweise sogar mehr als die Fibrillen.
„Härchen aggregation beginnt mit der Keimbildung, gefolgt von einer Dehnung der Bühne“, erklärt Kichitaro Nakajima, Blei-Autor der Studie. „Bis jetzt, die frühen Stadien von oligomer Entwicklung schwierig gewesen, zu studieren, wegen Ihrer morphologischen Variabilität der Zeitraum für die Keimbildung und das fehlen eines geeigneten fluoreszierenden assay.“

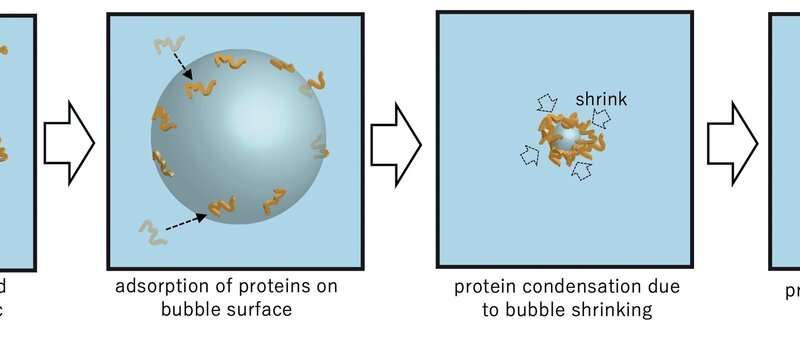
Mit flüssig-Zustand Transmissions-Elektronen-Mikroskopie konnten die Forscher analysierten die aggregation der Proteinmoleküle, den Erwerb von time-resolved nanoskaligen Bilder und Elektronen-Beugungsmuster. „Bemerkenswert ist, dass wir entdeckt, dass eine Salz-Kristall ausfallen kann, auch bei einer Konzentration weit unterhalb Ihrer Löslichkeit aufgrund der lokalen-Dichte-Fluktuation und der schnellen Auflösung beschleunigt die aggregation Reaktion von amyloid-β-Peptiden“, sagt Professor Hirotsugu Ogi, der entsprechende Autor. „Dieser Bildung von temporären Salzkristalle bietet einen Mechanismus, durch den Proteine haften an der Oberfläche des Kristalls; als es sich auflöst, die Oberfläche schrumpft, wobei die Proteine auf den Fluchtpunkt zu. Dieses Phänomen ähnelt der aggregation Beschleunigung durch Ultraschall cavitation bubble. Proteine sind an der Blase an der Oberfläche während der ausbau-phase, und Sie sind hoch verdichtet durch die nachfolgende Blase kollabiert der positive Druck der Ultraschall-Welle in der Mitte. Dies ist die künstliche katalytische Wirkung. Also, in eine Autokatalytische-wie nanoskopischen aggregation Mechanismus, Salz-Auflösung, beschleunigt die aggregation Reaktion, und das Aggregat selbst fördern kann Salz Keimbildung.“
