Die Bauchspeicheldrüse ist ein abdominal-organ, produziert Verdauungsenzyme sowie die Hormone, die regulieren den Blutzuckerspiegel. Diese hormonproduzierenden Funktion lokalisiert ist, um die Langerhans-Inseln, die als Cluster von verschiedenen endokrinen Zelltypen. Unter denen, die die beta-Zellen, die das Hormon insulin benötigt, um niedriger Glukose (eine Art Zucker) – Spiegel in unserem Blut, als auch die alpha-Zellen, die erzeugen das Hormon glucagon verantwortlich für die Anhebung des Blutzuckerspiegels im Blut.
Typ-1-diabetes ist eine chronische Erkrankung, bei der das körpereigene Immunsystem fälschlicherweise angreift und zerstört die Bauchspeicheldrüse insulin-produzierenden beta-Zellen. Die Regenerative Medizin zielt darauf ab, Sie wieder aufzufüllen beta-Zell-Masse und damit der Unterstützung ersetzen, und schließlich die aktuelle insulin-Ersatz-Therapien. Änderungen zu Insel Zusammensetzung, einschließlich Unzureichende beta-Zellfunktion und beta-Zell-dedifferention, auch dazu beitragen, Typ-II-diabetes. Daher, ein tieferes Verständnis für die Identität und das übersprechen der verschiedenen inselzell-Arten führt zu einer besseren Charakterisierung der beiden Formen von diabetes, und kann dazu beitragen, die Entwicklung neuer therapeutischer Konzepte.
Single-cell-transcriptomics ist eine leistungsstarke Technik zur Charakterisierung zellulärer Identität. Zuvor, CeMM-Forscher von Christoph Bock und Stefan Kubicek Gruppen am CeMM veröffentlicht, die erste single-Zell-transkriptoms von primären humanen Pankreas-Inselzellen (EMBO Rep). Fortschritte in der Technologie haben seit aktiviert Ihre Anwendung auf die generation der globalen menschlichen und Maus einzelne Zelle Transkriptom-Atlanten. Trotz dieser Fortschritte, einzelne Zelle, die Ansätze bleiben technologisch anspruchsvolle gegeben, dass winzige RNA-Menge vorhanden ist gänzlich aufgebraucht im experiment. Es ist daher unabdingbar, um die Qualität und die Reinheit des resultierenden Einzel-Zell-transkriptoms.
CeMM-Forscher in den beiden Beitrag Laboratorien ermittelten unerwartet hohen Hormon-expression in nicht-endokrinen Zelltypen, sowohl im eigenen Datenbestand als auch andere in der Website veröffentlichten Einzel-Zell-Studien. Sie legen dar, um zu klären, ob dies wäre die Folge der Verunreinigung durch RNA-Moleküle, zum Beispiel von absterbenden Zellen, und, wie könnte es entfernt werden, um ein zuverlässiges dataset. Eine solche Verunreinigung scheint vorhanden in der einzelnen Zelle RNA-seq-Daten aus den meisten Geweben wurde aber am deutlichsten in Pankreas-Inseln. Insel endokrinen Zellen sind ausschließlich gewidmet der Produktion einzelner Hormone und insulin in beta-Zellen und glucagon in den alpha-Zellen exprimiert werden, zu höheren Ebenen, als typische „housekeeping“ Gene. Also, Umverteilung von dieser Transkripte zu anderen Zelltypen war sehr ausgeprägt. Auf dieser Beobachtung basiert, Ihr Ziel war die Entwicklung, Validierung und Anwendung einer Methode experimentell zu bestimmen und rechnerisch zu entfernen, wie Kontamination.
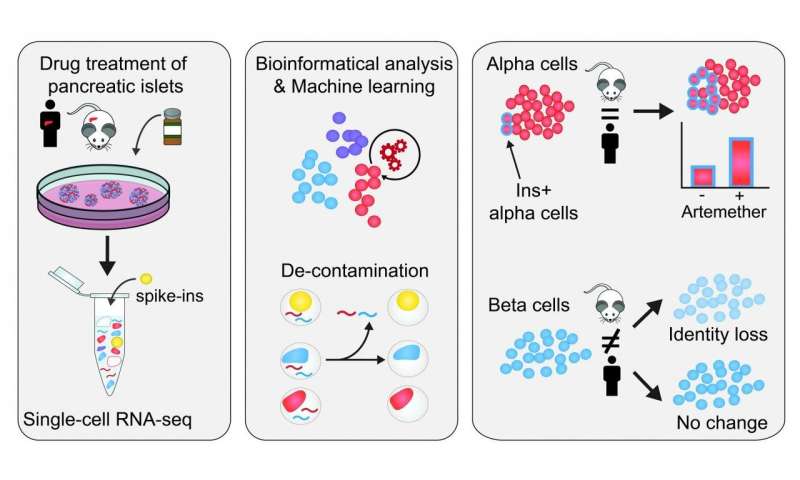
In Ihrer Untersuchung, CeMM-Forscher verwendeten Spike-in Zellen aus unterschiedlichen Zelltypen, die sowohl Maus-und menschlichen Proben, dass Sie Hinzugefügt, um Ihre pancreatic islet Proben. Wichtig ist, die transkriptome von diesen spike-in Zelle wurden vollständig charakterisiert. Dieses erlaubt Ihnen, zu Steuern, intern und passgenau auf der Ebene der RNA-Kontamination in den einzelnen Zelle, die RNA-seq, dass die menschliche Transkripte erkannt und die Maus spike-in Zellen darstellen Kontamination der RNA. Auf diese Weise fanden Sie, dass die Proben hatten ein Verschmutzungsgrad von bis zu 20%, und waren in der Lage zu definieren, die Kontamination in den einzelnen Proben. Sie dann entwickelt eine neuartige Bioinformatik-Ansatz, rechnerisch zu entfernen, zu verunreinigen liest aus Einzel-Zell-transkriptoms.
Jetzt haben, erhalten ein „dekontaminiert“ Transkriptom, aus dem das Störsignal entfernt worden ist, ging Sie zu charakterisieren, wie die zelluläre Identität in den verschiedenen Zelltypen reagierten auf die Behandlung mit drei verschiedenen Medikamenten. Sie fanden heraus, dass ein niedermolekularer inhibitor des transkriptionsfaktors FOXO1 induziert entdifferenzierung der beiden alpha-und beta-Zellen. Darüber hinaus untersuchten Sie artemether, die gefunden worden verringern und die Funktion der alpha-Zellen und induzieren könnte insulin-Produktion in in-vivo-und in-vitro-Studien (Zelle). Die Wirkung der Droge artemether waren Spezies-spezifisch und cell-type-specific. In der alpha-Zellen, in einem Teil der Zellen erhöht die insulin-expression und gewinnen Aspekte der beta-Zell-Identität, sowohl in der Maus und humanen Proben. Wichtig fanden die Forscher, dass in menschlichen beta-Zellen, es gibt keine signifikanten Veränderungen in der insulin-expression, wohingegen in der Maus Inselchen beta-Zellen, verringern Sie Ihre insulin-expression und Gesamt-beta-Zell-Identität.
