
Bridging integrator 1, bekannt als BIN1, ist der zweithäufigste Risikofaktor für late-onset Alzheimer-Krankheit, nach der Genom-weiten Studien von genetischen Varianten. Doch die Wissenschaftler wissen wenig über das, was dieses protein im Gehirn.
Jetzt hat eine neue präklinische Studie hat entdeckt, dass ein Mangel an BIN1 führt zu einem defekt bei der übertragung von Neurotransmittern, aktivieren die Gehirn-Zell-Kommunikation ermöglicht es uns, zu denken, erinnern und Verhalten. Angeführt von Gopal Thinakaran, Ph. D., von der University of South Florida Health (USF Health) Morsani College of Medicine, und Kollegen an der Universität von Chicago, die Studie wurde veröffentlicht im März 10 in Cell Reports.
Etwa 40% der Menschen mit Alzheimer-Krankheit eine von drei Varianten in der BIN1-gen—ein glitch in einem einzigen DNA-Baustein (Nukleotid), das erhöht Ihr Risiko für die neurodegenerative Erkrankung, sagte der Studie leitende Autor Dr. Thinakaran, ein professor der molekularen Medizin an der USF Health Byrd Alzheimer ‚ s Center und associate dean für die neurowissenschaftliche Forschung an der Morsani College of Medicine.
„Unsere Ergebnisse, dass BIN1 lokalisiert direkt am point of präsynaptischen Kommunikation und kann genau das sein, der Regulierung der neurotransmitter vesicle release bringt uns näher zum Verständnis, wie BIN1 ausüben könnte seine Funktion als gemeinsamer Risikofaktor für die Alzheimer-Krankheit,“ Dr. Thinakaran sagte. „Wir vermuten, es hilft bei der Kontrolle, wie effizient Neuronen kommunizieren und kann tiefgreifende Auswirkungen auf die Speicher-Konsolidierung—Prozess, verwandelt den letzten Erfahrungen gelernt in long-term memory.“
Das research team erstellt, einem Maus-Modell, in dem die BIN1-gen wurde selektiv inaktiviert, oder heraus geklopft werden, um zu charakterisieren das protein die normale Funktion im Gehirn. Insbesondere, Sie verwendet fortgeschrittene Zell-und molekularbiologischer Techniken zur Untersuchung der Rolle von BIN1 bei der Regulierung der Synapsen im Zusammenhang mit lernen und Gedächtnis.
Rahmen die Ergebnisse der Studie, es hilft zu wissen, dass eine gesunde menschliche Gehirn enthält Milliarden von Gehirnzellen (Neuronen), die das Bearbeiten und übertragen von chemischen Nachrichten (Neurotransmitter), die über einen winzigen Spalt zwischen Neuronen genannt synapse. In der Alzheimer-Gehirn, das die synaptische Kommunikation ist zerstört, schrittweise töten Neuronen und letztlich verursachen eine steile Abnahme von Gedächtnis, sowie andere Anzeichen von Demenz. Individuen die meisten anfällig für die Entwicklung ausgewachsenen Alzheimer im späteren Leben sind diejenigen, die verlieren die meisten Synapsen, Dr. Thinakaran sagte.
Unter den Cell Reports study highlights:
- Verlust des BIN1-expression in Neuronen führt zu einer Beeinträchtigung des räumlichen Lernens und des Gedächtnisses. Das heißt, das Defizit verändert, wie effektiv Informationen über die umgebende Umwelt Raum erfasst, gespeichert, organisiert und genutzt werden. Die BIN1-knockout-Mäuse hatten signifikant mehr Schwierigkeiten als Steuerelemente zu finden, die versteckte Plattform im Morris water maze.
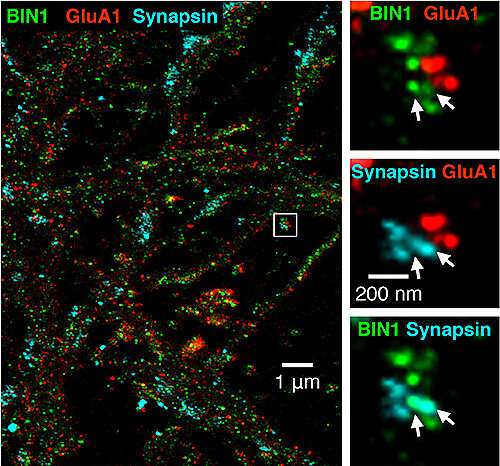
- Weitere Analysen unterschieden, dass BIN1 hauptsächlich lokalisiert auf Neuronen, die senden Neurotransmitter über die Synapsen (präsynaptische Seiten) statt, die sich auf jene Neuronen, die den neurotransmitter-Nachrichten (postsynaptischen Seiten). Die synaptische übertragung im hippocampus, einer Hirnregion, die in Erster Linie mit memory, zeigte eine Verschlechterung in der Freisetzung von Neurotransmittern aus Vesikeln. Vesikel sind blasenartige Fluggesellschaften, die übertragung von Neurotransmittern aus präsynaptischen zur postsynaptischen Neuronen.
- Die BIN1-Defizienz war assoziiert mit einer reduzierten Dichte der Synapsen und zu einer Abnahme in der Anzahl der synaptischen Cluster in den knockout-Mäusen im Vergleich zu Kontrollen.
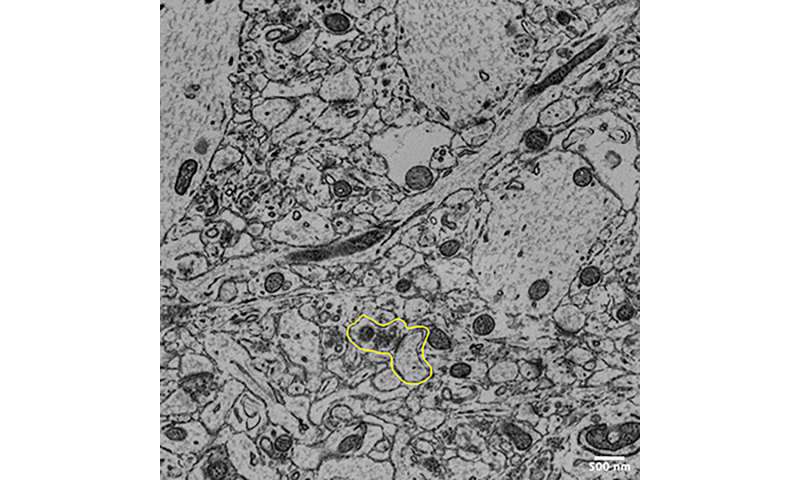
- 3-D-Elektronen-Mikroskopie Umbau der Synapsen zeigten eine signifikante Akkumulation von angedockt und reserve-pools synaptischer Vesikel in der BIN1-knockout-Mäuse. Das zeigt an, langsamer (weniger erfolgreich) die Freisetzung von Neurotransmittern aus Ihren Vesikeln, vermuten die Forscher.
